网络广告发展到今天,经历了从最初的短信联盟到现在的广告联盟,广告形式也有了很大的变化,出现了CPC、CPM、CPA、CPS、CPT等众多广告形式。今天就为大家科普这些广告术语,一次搞懂! 1. CPM:按展示付费 CPM—英文全称Cost Per Mille 或者是Cost Per ThousandImpression,…
美国FDA、OTC和NDC是什么?区别在哪里?三者有什么关系
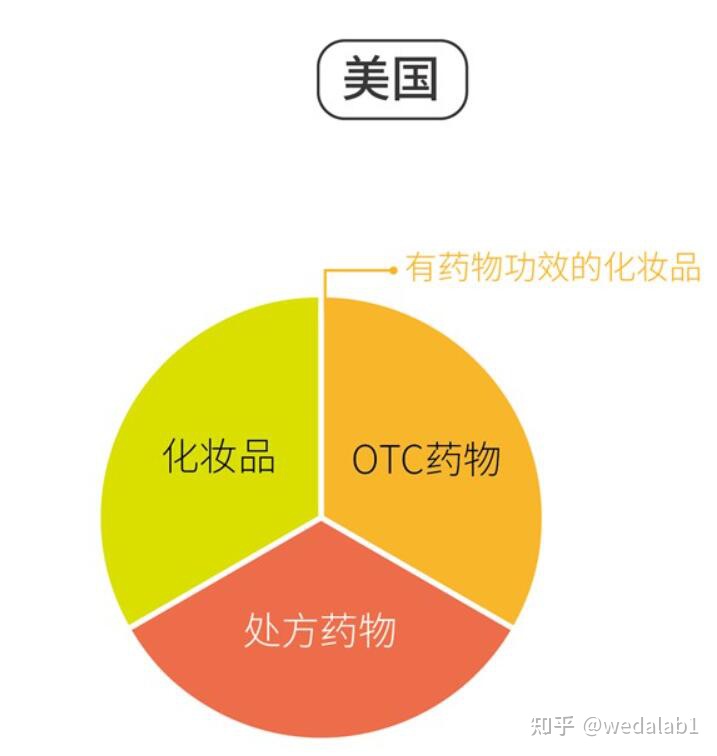
什么是FDA?
FDA是美国食品药品监督管理局(Food and Drug Administration)的简称,它是美国卫生与公众服务部直辖的联邦政府机构,是世界上最大的食品与药品关机机构之一,由社会各界的精英专业人士组成,包括医生、律师、微生物学家,化学家、统计学家等。
FDA认证是指,凡是美国本土生产及美国进口的食品、药品、化妆品都必须经过FDA的认证,只有经过FDA认证,进行了企业和产品信息办理备案的的产品才可以进入美国市场进行流通。
跨境电商卖家在进行FDA认证时,需提供产品资料、涉外工程师对产品资料进行的评估报价、卖家在签订合作协议后付款,填写申请表,完成注册后,就会收到FDA回执。
什么是NDC?
NDC(National Drug Code),指国家药品验证号,是药品作为普通商品的识别符号,是中国中药及OTC非处方药通过FDA认证的快捷申请形式。对于美国国家药典已经录入的药,不再需要做新药论证,产品在达到美国FDA各项法规保罗印刷文字及包装等方面的要求后,只需要提供必要的材料进行申请。
获得美国NDC的药品可以在中西方同时销售,相比申请国家新药(NDA)来说,减少了大量的时间和成本,市场前景也更好。
具有药准字号的中药及OTC非处方药品,可以直接申报美国NDC,这也是中国药品进入美国的一个好方法。
什么是OTC?
OTC(over the counter drug)是非处方药,指为方便公众用药,在确保用药安全的前提下,经国家卫生行政部门规定或审定后,公众凭自己对自己身体及病情的判断,不需要通过医师或其它医疗专业人员的诊断,自己就可以购买的药品。美国的非处方药均要注明“适应的用药指导”(Adequate Direction foruse)。
美国FDA要求非处方药必须标有7项信息:产品名称;生产商、包装商或分发商的名称;地址;包装内容物;所有有效成份的INN(国际非专利药物通用名)名称;某些其它组分如乙醇、生物碱等的含量;保护消费者的注意事项及忠告性内容;安全、正确使用该药品适当的用药指导。
三者的关系
简单来说,三者的关系如下:
FDA是美国食品药品药监局,FDA认证是食品药品进入市场必须要经过的步骤,NDC是FDA监管下的一个类别,OTC是中国的叫法,其实就是美国的NDC。
实例:
FDA是美国食药监局,也就是大家所说的FDA认证,实际并不叫FDA认证,NDC是FDA监管的的其中的一个类别而已,所以有很多朋友叫FDA认证,严格来讲是叫NDC,那么另外有很多朋友叫OTC,OTC是中国的叫法,美国NDC 也就是中国大家叫的OTC(非处方药)。 只有人体消毒液等产品才是做OTC,如果是物品空气消毒那需要做EPA,是另外一个认证
国家药品验证号(NDC)是中国中药及OTC非处方药通过FDA认证的快捷申请形式。主要针对美国国家药典已有的药,无需做新药论证,只需提供必要的材料进行申请,但要求较严,必须达到美国FDA的各项法规,包括印刷文字及包装。获得美国NDC的药品可在中西药房销售,这类药物在市场获利颇丰,且比申请国家新药(NDA)花费的时间和成本大大减缩。中国具有药准字号的中药及OTC非处方药产品皆可申报美国NDC,可以说是中药及OTC非处方药进入美国的一条很好的途径。
在美国,免洗消毒洗手液属于局部消毒的非处方药(OTC,Over-the-Counter),与去屑洗发水、含氟牙膏、防晒霜等产品一样,受食品药品监督管理局(FDA) 监管。虽然属于药品类,但大部分OTC产品的合规要求还是比较简单的。
一般来说,FDA会统一审查用于OTC药品的活性成分,并最终出具一份OTC专论(OTC Monograph)。OTC专论就相当于活性物质标准,对于OTC产品,只要其中的活性成分满足OTC专论的要求,就可以不经FDA审批直接上市。美国FDA,OTC,NDC三者区别
需要注意,不用FDA审批并不意味着OTC药品上市没有任何合规义务,产品仍旧需要满足一定的要求,具体的要求如下:
1.OTC药品里的活性成分必须有现成的OTC专论,并且企业所用的活性成分符合OTC专论的要求,否则产品就要做OTC新药申请;对含酒精的免洗消毒洗手液来说,酒精在美国已经有相应的OTC专论,所以只要用于生产的酒精满足专论的要求,产品上市就可以不用经过FDA审批了。
2.OTC药品的生产商或进出口商必须进行FDA厂址登记,对美国境外的企业来说,则需要委托美国境内的代理进行FDA厂址登记。
3.为OTC药品申请一个国家药品编号(NDA, National Drug Code) 。
4.企业必须把将要进入美国市场的所有OTC药品列出清单并在FDA进行备份,之后此清单每年至少要在6月和12月更新两次。
5.OTC药品的标签必须符合相应的标签规定。
6.生产工厂必须满足动态药品生产管理规范(cGMP) 的要
人体用洗手液,消毒液,消毒湿巾等所需资料:
营业执照,拍公章的照片(盖印那一面朝上),邓白氏申请表,产品信息表,otc药pin注册申请表。
周期是所有资料提交完之后3-4周
免洗洗手液的FDA-NDC(OTC)注册流程和费用如下:
1、先向邓白氏申请邓白氏编码(DUNS),邓白氏编码免费的要一个月,付费的一个礼拜内可以下来(收费是800人民币,这个费用是由客户直接付给邓白氏),大家可以百度搜索华夏邓白氏。或者也可以咨询我
2.企业注册
3.产品注册
本文:美国FDA、OTC和NDC是什么?区别在哪里?三者有什么关系
![]()